Essa questão aborda a análise das fórmulas estrutural e de Lewis (eletrônica) de três substâncias comuns no nosso dia a dia: a água, o oxigênio, e água oxigenada. Vamos relembrar o que são essas representações:
➯ Estrutura eletrônica de Lewis: é uma representação que leva em consideração os elétrons da camada de valência e os representa em cada átomo. Os elétrons compartilhados que formam a ligação são circulados, e os elétrons livres são representados ao redor da sigla do átomo. Esses elétrons são representados por bolinhas.
➯ Fórmula estrutural: é uma representação simplificada das ligações, em que o compartilhamento de elétrons é reduzido a um traço simples, e os elétrons livres não são representados. Cada traço simplifica uma ligação simples, ligações duplas ou triplas acumulam dois ou três traços.
Precisamos lembrar que representamos apenas a camada mais externa de elétrons dos átomos, a camada de valência.
Vamos às representações:
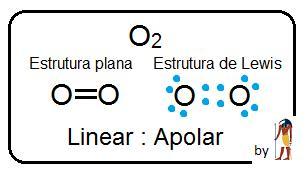
➯ O₂: 6 elétrons na valência
: :
Eletrônica: : O : : O :
: :
Estrutural: O = O
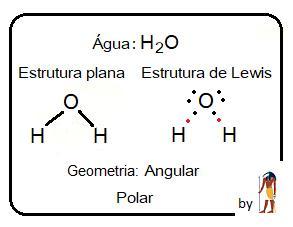
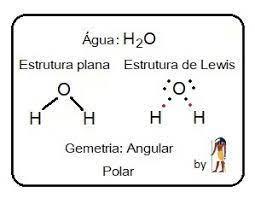
➯ H₂O: 1 elétrons na valência do hidrogênio e 6 na do oxigênio
:
Eletrônica: H . . O . . H
:
Estrutural: H – O – H
Existem um ângulo nessa representação que não dá pra ser representado aqui. Vou adicionar em anexo a representação original.
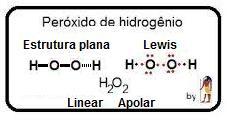
➯ H₂O₂:
: :
Eletrônica: H . . O . . O . . H
: :
Estrutural: H – O – O – H
*Créditos da foto ao Toth.
Saiba mais sobre fórmulas estruturais em:
https://brainly.com.br/tarefa/45662702
Espero ter ajudado!